Den udbredte brug af små husholdningsapparater blandt forbrugere medfører behov for strømkilder eller enkeltforsyningskredsløb galvaniske celler, almindeligvis kendt som batterier. De opstod første gang i 1800 takket være den italienske fysiker Alessandro Volta. De varierer i størrelse og form, spænding, kapacitet og batteritype. Alkaliske og saltvandsbatterier anvendes i vid udstrækning på markedet for små husholdningsapparater og elektronik.
Hvad er saltvandsbatterier?
Saltbatterier — kilder til elektrisk strøm genereret i en simpel enhed gennem en kemisk reaktion. De kaldes undertiden kulstof-zink-batterier eller kulstofbatterier. Denne type celle betragtes som den billigste, men har en lav energitæthed, hvilket gør den velegnet til enheder med lavt strømforbrug. I enheder med højt strømforbrug eller med karakteristiske stigninger i belastningsstrøm og temperatur holder de ikke længe og bruges derfor ikke.
Betegnelse af saltbatterier
Betegnelsen for saltvandsbatterier accepteres i henhold til flere standarder:
- Amerikansk klassifikationssystem.
- Internationalt system (IEC).
- Mellemstatslig standard (GOST).
| Amerikansk klassifikationssystem | International klassificering IEC | GOST | Størrelse, mm | Kapacitet, mAh |
| EN | R23 | 17x50 | ||
| AA | R6 | 316 | 14,5x50,5 | 1100 |
| AAA | R03 | 286 | 10,5x44,5 | 540 |
| C | R14 | 343 | 26,2x50 | 3800 |
| D | R20 | 373 | 34,2x61,5 | 8000 |
| F | 25 kr. | 33x91 | ||
| 1/2AA | 14250 kr. | 312 | 14,5x25 | 250 |
| R10 | R10 | 332 | 21,5x37,3 | 1800 |
For eksempel betyder mærkningen af et saltvandsbatteri R 6: rund, cylindrisk, finger, salttypeelement, samlede dimensioner 14,5x50,5, kapacitet1100 mAh. Standardspændingen er 1,5 V. "R"-betegnelsen (salt) på batterimærket adskiller saltbatterier fra andre typer batterier (alkaliske eller lithium).
Design og komposition
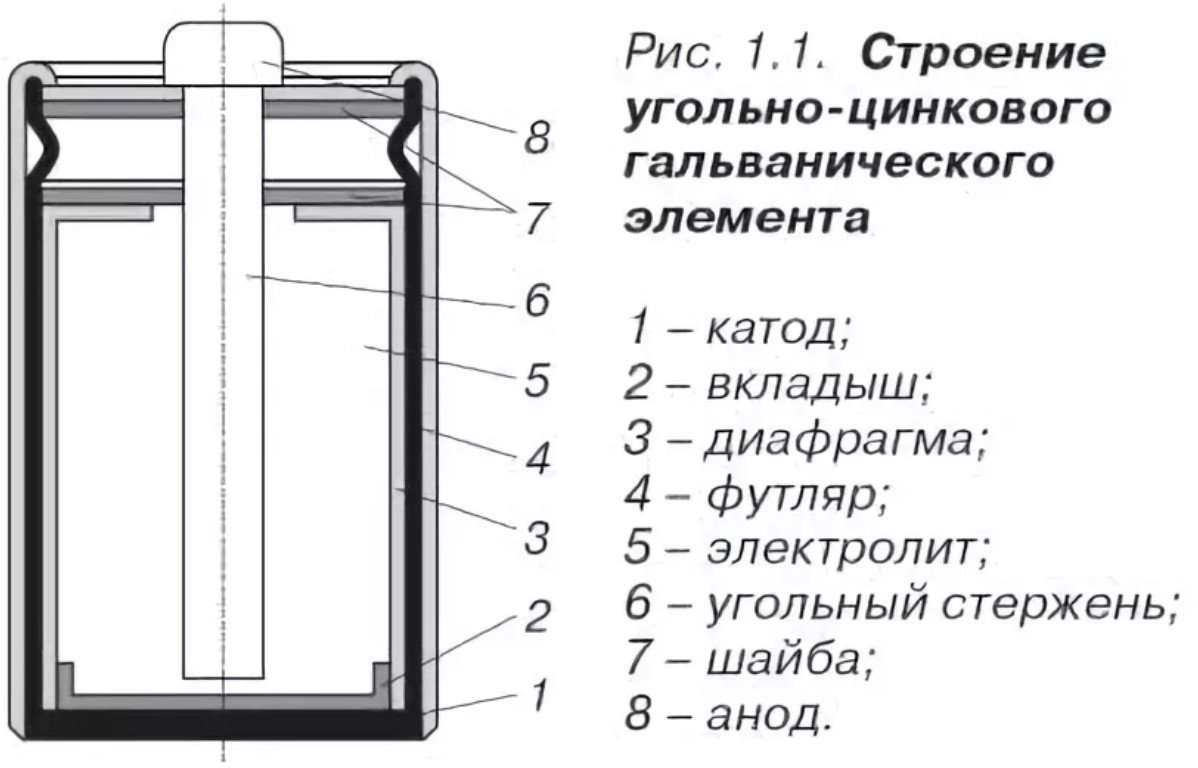
Designet af et saltbatteri er ret simpelt og består af:
- Katode - den samme Saltbatteriets hus er lavet lavet af zink, med forbedrede korrosionsbestandige egenskaber og en høj rensningsgrad (minus).
- Anoden er et agglomerat, fremstillet ved presning, imprægneret med elektrolyt (plus).
- Elektrolyt: ammoniumchlorid eller zinkchlorid, med tilsætning af et fortykningsmiddel (stivelse).
- Kulstrømleder - løber gennem midten, behandlet med paraffinsammensætning.
- Gaskammer - placeret øverst, designet til at opsamle gasser fra den kemiske reaktion.
- Pakning - placeret øverst, fungerer som tætningsmiddel.
- Beskyttelsesetui - pap eller blik til beskyttelse mod korrosion og elektrolytlækager.
Lad os betragte sammensætningen af et saltbatteri fra et kemisk synspunkt:
- Katoden er højt renset zink, der er modstandsdygtig over for korrosion.
- Anode - MnO blanding2, grafit, elektrolytimprægnering.
- Elektrolytten er ammoniumchlorid eller en blanding af zinkchlorid og calciumchlorid.
Hvilke batterier er bedre: saltvand (1) eller alkaliske (2)?
Sammenligningen kan foretages i form af en tabel, hvor fordele og ulemper ved forskellige typer elementer tydeligt fremgår:
| Sammenligningsparametre | 1 | 2 |
| Temperaturforhold, driftsforhold | Ydelsen reduceres ved lave temperaturer og kan ikke modstå strømstigninger. | Fungerer godt ved lave temperaturer - ned til -20Åh, modstår let overspændinger, er ikke bange for en kraftig stigning i belastningsstrømmen |
| Bedst før-dato | 2-3 år | 5 år |
| Anvendelse | Velegnet til brug i enheder med lavt strømforbrug | Velegnet til brug i udstyr med mellemstort og højt energiforbrug |
| Instrumenter, tekniske apparater | Vækkeure, vægure, fjernbetjeninger, mini-lommelygter, simpelt legetøj | Afspillere, lommelygter, musiklegetøj, stemmeoptagere, blodtryksmålere |
Når du vælger en strømkilde til en enhed med specifikke driftskrav, er det vigtigt at vide, hvordan man skelner mellem et saltvandsbatteri og et alkalisk batteri. Saltvandsbatterier er markeret med bogstavet R, mens alkaliske batterier er efterfulgt af bogstavet L (LR).
Konklusioner og anbefalinger
Denne type strømkilde er lettere og mere overkommelig. Saltvandsbatteriers holdbarhed er dog kort – 2 til 3 år – og de kan undergå delvis selvafladning under opbevaring og under brug under en pludselig strømstigning. Derfor er det, på grund af deres relativt dårlige ydeevne, men relativt lave pris, nemt at købe flere sæt batterier som backup.
Ikke høj kapacitetsaltbatterier (2-3 gange mindre end andre typer) begrænser deres anvendelse til simple enheder med lav belastningsstrøm.
Det er nemt at afgøre, om det er muligt at oplade saltvandsbatterier: batteriets navn er angivet på enhedens kabinet, der er beregnet til opladning. kapacitetI mAh. Hvis denne værdi ikke er tilgængelig, er det et almindeligt batteri, og på trods af adskillige ekspertråd bør det ikke oplades. Opladning vil ikke give den forventede langsigtede effekt og kan føre til en ulykke på grund af overophedning og elektrolytlækage. Hvis du har brug for en mere pålidelig og holdbar strømkilde, er det bedre at investere i et alkalisk alternativ eller et genopladeligt batteri.
Interessant faktum: Gør-det-selv saltbatteri Det kan laves meget simpelt. Du skal bruge 50-kopek-mønter, folie, papir og en saltopløsning. Det er bedst at lægge mønterne i blød i en eddikeopløsning før brug for at fjerne plak eller snavs. Saml enheden: en mønt, papir dyppet i saltopløsningen og folie. Gentag denne proces flere gange, og lav en søjle med mønten (positiv) i den ene ende og folien (negativ) i den anden. Strøm genereres af den potentielle forskel, der skabes af elektrolytten (saltopløsningen) mellem foliens metal og mønten. Denne opfindelse kaldes en voltaisk bunke, og dens spænding afhænger direkte af antallet af anvendte mønter: jo flere mønter der er, desto højere er den opnåede spænding. Men efter eksperimentet er mønterne ikke længere brugbare; de vil have en rusten belægning.